Zjawiska chemiczne stanowią fundamentalną część procesów zachodzących w otaczającym nas świecie. Są to procesy prowadzące do powstania nowych substancji poprzez przemianę substratów w produkty. W przeciwieństwie do zjawisk fizycznych, podczas reakcji chemicznej następuje zmiana w strukturze cząsteczek - wiązania chemiczne są zrywane i tworzone na nowo.
Każda reakcja chemiczna wymaga spełnienia określonych warunków. Mogą one zachodzić z wydzieleniem lub pochłonięciem energii, najczęściej w postaci ciepła. Te procesy są wszechobecne w naszym codziennym życiu - od spalania świecy po pieczenie ciasta.
Najważniejsze informacje:- Reakcje chemiczne tworzą nowe substancje o innych właściwościach
- Podczas reakcji następuje rozerwanie i utworzenie nowych wiązań chemicznych
- Reakcje mogą zachodzić z wymianą energii
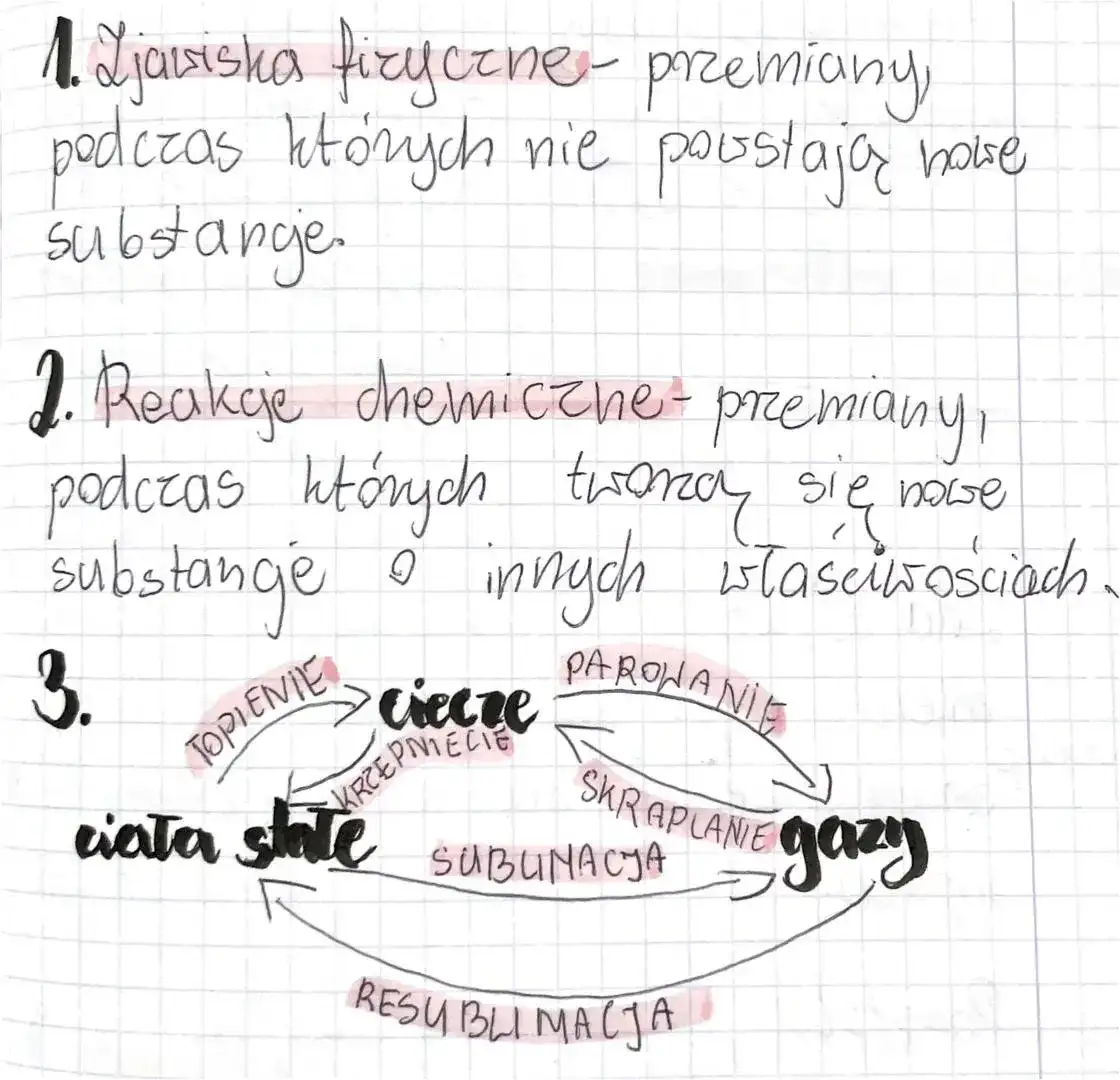
- Zjawiska chemiczne różnią się od fizycznych zmianą struktury substancji
- Wyróżniamy reakcje syntezy, analizy, wymiany i spalania
- Procesy chemiczne są powszechne w życiu codziennym
Czym są zjawiska chemiczne?
Zjawiska chemiczne to fundamentalne procesy zachodzące w otaczającej nas rzeczywistości. Podczas przemiany chemicznej dochodzi do powstania zupełnie nowych substancji. Te fascynujące transformacje towarzyszą nam każdego dnia, choć nie zawsze zdajemy sobie z tego sprawę.
Każde zjawisko chemiczne wiąże się z przemianą materii na poziomie cząsteczkowym. Reakcje chemiczne prowadzą do powstania produktów o innych właściwościach niż substancje wyjściowe. Podczas tych procesów następuje rozrywanie i tworzenie nowych wiązań między atomami.
Charakterystyka reakcji chemicznych
Reakcje chemiczne zachodzą, gdy dochodzi do przemian na poziomie wiązań chemicznych. Substancje wyjściowe, zwane substratami, przekształcają się w nowe związki - produkty.
Każda przemiana chemiczna wymaga określonych warunków do zajścia. Temperatura, ciśnienie i obecność katalizatorów mogą wpływać na szybkość i przebieg reakcji.
Procesy chemiczne mogą zachodzić samorzutnie lub wymagać dostarczenia energii. W naturze występują zarówno reakcje gwałtowne, jak i powolne przemiany materii.
- Nieodwracalna zmiana właściwości substancji
- Powstawanie nowych związków chemicznych
- Wymiana energii z otoczeniem
- Zachowanie zasady zachowania masy
- Określona stechiometria reagentów
Energia w reakcjach chemicznych
Energia odgrywa kluczową rolę w reakcjach chemicznych. Podczas przemian może być pochłaniana lub wydzielana w różnych formach. Najczęściej obserwujemy wymianę energii w postaci ciepła.
Niektóre reakcje chemiczne wymagają dostarczenia energii, by mogły zajść. Inne z kolei uwalniają energię do otoczenia. Kontrola przepływu energii jest kluczowa w procesach przemysłowych.
| Typ przemiany | Energia | Przykład |
| Egzotermiczna | Wydzielanie | Spalanie węgla |
| Endotermiczna | Pochłanianie | Fotosynteza |
Czytaj więcej: Marynowane papryczki jalapeno - przepis na marynatę idealną na zimę
Podstawowe typy reakcji chemicznych
Reakcje chemiczne można podzielić na kilka podstawowych typów. Każdy typ charakteryzuje się specyficznym mechanizmem przemiany substratów w produkty.
Znajomość rodzajów reakcji chemicznych pomaga zrozumieć procesy zachodzące w przyrodzie. Pozwala też przewidzieć produkty reakcji.
- Reakcje syntezy - łączenie prostszych substancji w bardziej złożone
- Reakcje analizy - rozkład związków na prostsze substancje
- Reakcje wymiany - wymiana atomów lub grup atomów między reagentami
- Reakcje spalania - reakcje z tlenem z wydzieleniem energii
Reakcje syntezy i analizy
Reakcje syntezy to procesy łączenia się dwóch lub więcej substancji w jeden produkt. W przemyśle chemicznym są one podstawą produkcji wielu związków.
Reakcje analizy zachodzą, gdy jedna substancja rozpada się na prostsze składniki. Przykładem jest rozkład węglanu wapnia na tlenek wapnia i dwutlenek węgla.
W życiu codziennym spotykamy te reakcje np. podczas rdzewienia metali (synteza) czy rozkładu nadtlenku wodoru w wybielaczach (analiza). Te przemiany chemiczne są kluczowe w wielu procesach przemysłowych.
Reakcje wymiany i spalania
Reakcje wymiany polegają na zamianie miejscami atomów lub grup atomów między reagentami. Zachodzą one między roztworami elektrolitów.
Szczególnie ważne są reakcje spalania, podczas których substancje reagują z tlenem. Wydzielają one energię w postaci ciepła i światła.
W praktyce reakcje pierwiastków typu spalanie wykorzystujemy w silnikach spalinowych. Reakcje związków chemicznych typu wymiana są podstawą procesów oczyszczania wody.
Zjawiska chemiczne w życiu codziennym

Zjawiska chemiczne towarzyszą nam na każdym kroku. Korozja metali, fermentacja ciasta czy fotosynteza to tylko niektóre przykłady. Te naturalne procesy kształtują nasze otoczenie.
W kuchni zachodzi wiele reakcji chemicznych. Podczas gotowania, pieczenia czy smażenia substancje ulegają różnym przemianom. Zmienia się nie tylko ich wygląd, ale też właściwości.
Nawet oddychanie to seria skomplikowanych procesów chemicznych. W naszym organizmie nieustannie zachodzą reakcje metaboliczne. Są one niezbędne do życia.
| Zjawisko | Przykład | Obserwowane zmiany |
| Korozja | Rdzewienie metali | Zmiana koloru, struktura powierzchni |
| Fermentacja | Kiszenie ogórków | Zmiana smaku, konsystencji |
| Spalanie | Palenie świecy | Wydzielanie ciepła, światła |
| Fotosynteza | Produkcja tlenu przez rośliny | Wzrost rośliny, wydzielanie tlenu |
| Trawienie | Rozkład pokarmu | Zmiana struktury chemicznej |
Różnice między zjawiskami chemicznymi a fizycznymi
Zjawiska chemiczne różnią się fundamentalnie od zjawisk fizycznych. Podczas gdy te pierwsze prowadzą do powstania nowych substancji, zjawiska fizyczne zmieniają tylko formę lub stan skupienia materii.
W przemianach chemicznych następuje rozerwanie i utworzenie nowych wiązań między atomami. Natomiast w zjawiskach fizycznych struktura cząsteczkowa pozostaje niezmieniona.
Topnienie lodu to przykład zjawiska fizycznego - woda zmienia tylko stan skupienia. Z kolei rdzewienie żelaza to zjawisko chemiczne, bo powstaje nowa substancja o innych właściwościach.
Po reakcji chemicznej nie da się w prosty sposób odzyskać substancji wyjściowych. W przeciwieństwie do tego, zmiany fizyczne są zazwyczaj odwracalne.
Kiedy zachodzi przemiana chemiczna?
Przemiana chemiczna często daje wyraźne sygnały swojego zachodzenia. Możemy zaobserwować zmianę barwy, wydzielanie gazu lub powstawanie osadu. Podczas reakcji często następuje też wymiana energii z otoczeniem.
Obserwacja zmian zachodzących w substancjach pozwala określić rodzaj przemiany. Zmiana smaku, zapachu czy właściwości chemicznych świadczy o zajściu reakcji chemicznej. Najlepszym dowodem jest powstanie nowej substancji o innych właściwościach.
Znaczenie zjawisk chemicznych w przyrodzie
Zjawiska chemiczne są fundamentem życia na Ziemi. Fotosynteza, oddychanie komórkowe i rozkład materii organicznej to podstawowe procesy podtrzymujące życie. Bez tych reakcji egzystencja organizmów byłaby niemożliwa.
W przyrodzie przemiany chemiczne występują w cyklach biogeochemicznych. Obieg węgla, azotu i innych pierwiastków opiera się na serii reakcji chemicznych. Te naturalne procesy zapewniają równowagę w ekosystemach.
Nawet formowanie się skał i minerałów zachodzi dzięki procesom chemicznym. Wietrzenie chemiczne, krystalizacja i reakcje w głębi Ziemi kształtują powierzchnię naszej planety. Natura nieustannie przeprowadza skomplikowane reakcje na wielką skalę.
Fascynujący świat przemian chemicznych - od teorii do praktyki
Zjawiska chemiczne stanowią nieodłączną część naszego codziennego życia, od prostych reakcji w kuchni po skomplikowane procesy przemysłowe. Zrozumienie ich natury pozwala lepiej pojąć otaczający nas świat i procesy w nim zachodzące.Każda reakcja chemiczna to precyzyjnie określony proces, podczas którego powstają nowe substancje o odmiennych właściwościach. Te przemiany chemiczne możemy obserwować poprzez zmiany barwy, wydzielanie ciepła czy powstawanie osadów - zjawiska te są kluczowe dla funkcjonowania życia na Ziemi.
Różnorodność procesów chemicznych - od syntezy przez analizę po reakcje wymiany i spalania - tworzy fascynującą sieć zależności w przyrodzie. To właśnie dzięki nim możliwe jest zachowanie równowagi w ekosystemach i rozwój życia w takiej formie, jaką znamy.