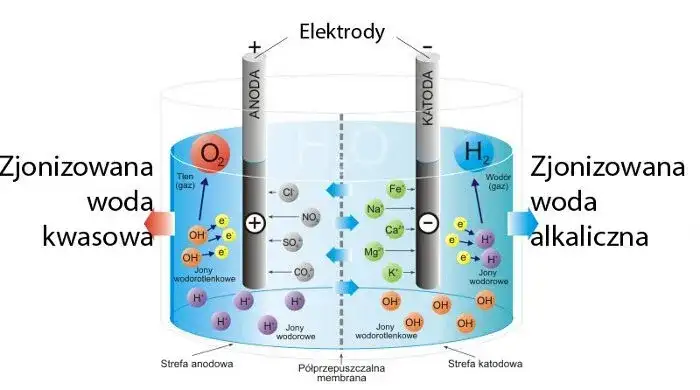
- Elektroliza przekształca energię elektryczną w energię chemiczną.
- W procesie biorą udział elektrody oraz elektrolity, które umożliwiają przepływ prądu.
- Na anodzie zachodzi utlenianie, a na katodzie redukcja substancji chemicznych.
- Prawa Faradaya określają ilość wydzielających się substancji w zależności od przepływającego ładunku elektrycznego.
- Elektroliza ma zastosowanie w produkcji metali, takich jak aluminium i miedź.
- Elektroliza wody produkuje wodór i tlen, co jest kluczowe w kontekście energii odnawialnej.
- Nowe badania i technologie w dziedzinie elektrolizy mogą zrewolucjonizować przemysł chemiczny.
- Wyzwania związane z elektrolizą obejmują koszty energii oraz efektywność procesów.
Czym jest elektroliza i jak działa?
Elektroliza to proces chemiczny, który przekształca energię elektryczną w energię chemiczną. W wyniku tego procesu substancje chemiczne są rozkładane na swoje składniki. Proces zachodzi w roztworach elektrolitów, które są substancjami zdolnymi do przewodzenia prądu elektrycznego. Główne elementy to elektrody oraz elektrolity, które pozwalają na przepływ prądu i umożliwiają zachodzenie reakcji chemicznych.W trakcie elektrolizy znajdują się dwie elektrody: anodowa (dodatnia) i katodowa (ujemna). Kiedy do układu przyłożone jest napięcie, kationy (jon dodatni) wędrują w stronę katody, a aniony (jon ujemny) dążą do anody. Ten ruch jonów jest kluczowy dla zachodzenia reakcji chemicznych, które prowadzą do wydzielania się różnych substancji na powierzchni elektrod.
Jakie są etapy elektrolizy?
Proces elektrolizy można podzielić na kilka kluczowych etapów. Pierwszym z nich jest przygotowanie roztworu elektrolitu, który musi być zdolny do przewodzenia prądu. Następnie do takiego roztworu wprowadza się elektrody, a na nie przyłożone zostaje napięcie. W tym momencie zaczyna zachodzić proces elektrolizy, którym sterują prawa chemiczne.
Główne etapy procesu elektrolizy to:
- Przygotowanie roztworu elektrolitu.
- Wprowadzenie elektrod do roztworu.
- Przyłożenie napięcia elektrycznego.
- Wydzielanie substancji na elektrodach.
Czytaj więcej: Najlepsze cytaty z Kubusia Puchatka i Prosiaczka o przyjaźni
Jakie reakcje zachodzą na elektrodach?
W procesie elektrolizy kluczową rolę odgrywają reakcje chemiczne, które zachodzą na anodzie i katodzie. Na anodzie, gdzie odbywa się utlenianie, dochodzi do utraty elektronów przez aniony. Przykładem może być reakcja wydzielania tlenu z wody, gdzie jony OH- oddają elektrony, a w efekcie powstaje tlen.
Na katodzie z kolei zachodzi redukcja, podczas której kationy przyjmują elektrony. Na przykład w procesie elektrolizy wody, spośród kationów H+ powstaje wodór. Takie reakcje są fundamentem zjawiska elektrolizy, które można zobaczyć w różnych zastosowaniach chemicznych.
| Rodzaj reakcji | Substancja wyjściowa | Produkt |
| Utlenianie | OH- | O2 |
| Redukcja | H+ | H2 |
Jakie są prawa elektrolizy Faradaya?
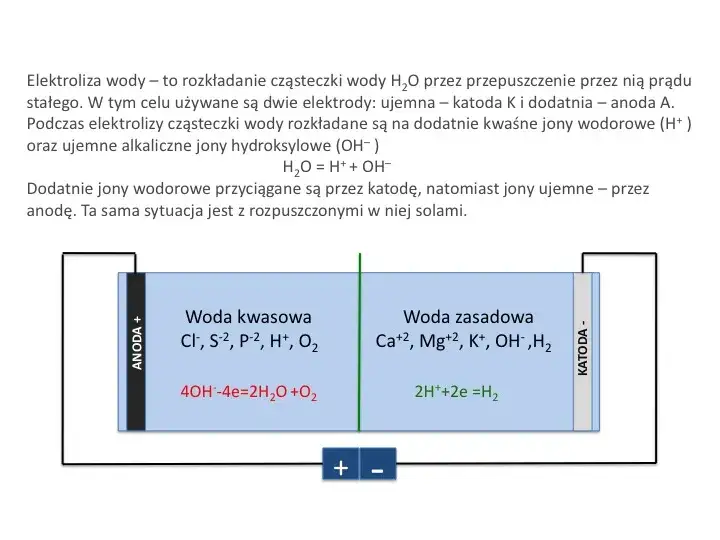
W kontekście zjawiska elektrolizy ważne są także prawa Faradaya, które wskazują na zależność między ilością ładunku elektrycznego a masą substancji wydzielającej się na elektrodach. Pierwsze prawo Faradaya mówi, że masa wydzielonej substancji jest proporcjonalna do ładunku przepływającego przez elektrolit. Oznacza to, że im więcej energii elektrycznej przechodzi przez układ, tym więcej substancji zostanie wyprodukowane.
Drugie prawo Faradaya stwierdza, że różne substancje wydzielają się w różnym stopniu przy tym samym ładunku. Prawo to ma znaczenie praktyczne, kiedy pracujemy z różnymi elektrolitami i substancjami chemicznymi, pozwalając przewidzieć, co się wydarzy podczas procesu elektrolizy.
Jakie są zastosowania elektrolizy w przemyśle?
Elektroliza ma ogromne znaczenie w przemyśle, a jej zastosowania są bardzo różnorodne. Dzięki elektrolizie uzyskuje się wiele ważnych surowców i produktów. Przykłady to produkcja metali, takich jak aluminium, sód czy miedź. Te metale są niezbędne w elektronice, budownictwie i wielu innych branżach.
Oprócz produkcji metali, zastosowania elektrolizy obejmują również wytwarzanie związków chemicznych, takich jak wodorotlenek sodu i kwas trifluorooctowy, a także produkcję gazów, takich jak wodór i tlen. Galwanizacja, czyli pokrywanie metali cienką warstwą innego metalu, również korzysta z tego procesu.
- Produkcja metali: aluminium, lit, sód.
- Produkcja związków chemicznych: NaOH, kwasy.
- Produkcja gazów: wodór, tlen.
- Galwanizacja: pokrywanie metalami.
Elektroliza wody: Jak powstaje wodór i tlen?
Jednym z najbardziej znanych zastosowań elektrolizy jest elektroliza wody, proces, w którym woda (H2O) jest rozkładana na wodór i tlen. Zachodzi on na katodzie i anodzie, przy czym wymaga przyłożenia napięcia wynoszącego co najmniej 1,229 V. Reakcja chemiczna przedstawia się następująco:
2H2O → 2H2 + O2
Na katodzie, gdzie odbywa się redukcja, powstaje wodór, natomiast na anodzie, w wyniku utleniania, wydziela się tlen. Proces ten ma ogromne znaczenie w kontekście produkcji zielonego wodoru, który jest kluczowym elementem strategii dekarbonizacji i przejścia na energię odnawialną.
Jakie są korzyści z użycia elektrolizy?
Wykorzystanie elektrolizy przynosi wiele korzyści. Przede wszystkim umożliwia produkcję czystych gazów, takich jak wodór i tlen, co ma znaczenie dla zrównoważonego rozwoju i zminimalizowania emisji CO2. Zjawisko elektrolizy pozwala także na efektywne uzyskiwanie metali oraz związków chemicznych, co przyczynia się do rozwoju przemysłu chemicznego i wydobywczego.
Dzięki nowoczesnym technologiom, proces ten staje się coraz bardziej efektywny i opłacalny. Na przykład, elektroliza wody może być zasilana energią ze źródeł odnawialnych, co czyni ją jeszcze bardziej ekologiczną. Przemiany te otwierają nowe możliwości w dziedzinie energii i ochrony środowiska.
Jakie są najnowsze trendy i badania związane z elektrolizą?
W dzisiejszych czasach elektroliza zyskuje na znaczeniu, a badania w tej dziedzinie organizowane są na całym świecie. Nowe technologie, takie jak elektrolizery o wysokiej wydajności, pozwalają na lepsze wykorzystanie energii elektrycznej oraz redukcję kosztów operacyjnych. Rozwój tych technologii może znacząco wpłynąć na różne sektory przemysłu, w tym na produkcję wodoru i metali.
Dodatkowo, naukowcy pracują nad nowymi elektrolitami, które poprawiają efektywność elektrolizy, a także nad metodami zrównoważonego rozwoju, które mogą zmniejszyć wpływ tego procesu na środowisko. Badania dotyczące materiałów używanych w elektrodach również pokazują obiecujące rezultaty, co może prowadzić do dalszego wzrostu efektywności procesu elektrolizy.
Jakie wyzwania są związane z procesem elektrolizy?
Pomimo wielu korzyści, zjawisko elektrolizy wiąże się także z pewnymi wyzwaniami. Przede wszystkim, koszty energii mogą być znaczące, co wpływa na opłacalność całego procesu. Dodatkowo, efektywność elektrolizy zależy od jakości używanych elektrolitów oraz elektrod. Zmniejszenie tych kosztów oraz zwiększenie efektywności to kluczowe wyzwania dla przemysłu.
Innym problemem jest również potrzeba dostosowania technologii do zmieniających się warunków rynkowych oraz zwiększenia zapotrzebowania na czyste źródła energii. Badania nad nowymi rozwiązaniami mają na celu przezwyciężenie tych trudności. Właściwe podejście do tych wyzwań może pomóc w dalszym rozwoju elektrolizy i jej zastosowań.
Elektroliza: Kluczowy proces przekształcania energii w chemii
Elektroliza to fascynujący proces, który umożliwia przekształcanie energii elektrycznej w energię chemiczną, prowadząc do rozkładu substancji na ich składniki. Dzięki odpowiedniemu zastosowaniu elektrolizy możliwe jest uzyskanie cennych gazów, takich jak wodór i tlen, a także produkcja metali i związków chemicznych, które mają kluczowe znaczenie w różnych branżach. W artykule omówiono mechanizmy działania elektrolizy, etapy tego procesu oraz prawa Faradaya, które wpływają na wydajność i efektywność reakcji.
Warto zwrócić uwagę na różnorodne zastosowania elektrolizy w przemyśle, w tym w produkcji zielonego wodoru, który odgrywa istotną rolę w dążeniu do zrównoważonego rozwoju i dekarbonizacji. Mimo licznych korzyści, proces ten nie jest wolny od wyzwań, takich jak wysokie koszty energii i potrzebę innowacji technologicznych. Zrozumienie tych kwestii jest kluczowe dla rozwoju zjawiska elektrolizy i jego zastosowania w aktualnych oraz przyszłych wyzwaniach energetycznych.
Podsumowując, elektroliza to nie tylko fundamentalny proces chemiczny, ale także przykład tego, jak energia elektryczna może być wykorzystywana do przekształcania substancji, przyczyniając się do nowoczesnych rozwiązań technologicznych i ochrony środowiska. W miarę jak świat dąży do większej efektywności energetycznej i zrównoważonego rozwoju, proces elektrolizy prawdopodobnie zyska na znaczeniu i stanie się jeszcze bardziej kluczowy w przyszłości.